射波刀(Cyberknife,也称为赛博刀)简介
一、射波刀的发展史
1988年,美国斯坦福大学从事放射外科治疗与研究的神经外科医生John Adler Jr博士提出了影像引导无框架立体定向放射外科的概念(iamge-guided frameless stereotactic radiosurgery)。随着计算机技术、神经导航技术和直线加速器放射外科的发展,1992年Adler及同事研制出最原始的无框架立体定向放射外科治疗设备,当时Adler将这种设备注册为Beta system (射波刀的雏形)。1994年射波刀开始治疗脑转移瘤患者。在以后的临床试用阶段,射波刀得到了进一步改进和完善,1999年美国FDA正式批准射波刀治疗系统 (Iamge-guided Cyberknife Radiosurgery / Radiotherapy System) 可用于治疗头部疾病,2001年美国FDA批准射波刀用于治疗全身肿瘤。尽管射波刀技术成熟,但是仍有诸多不完美之处。2002-2006年间,射波刀控制系统、剂量计划系统、靶区追踪系统、脊柱追踪技术、呼吸追踪技术进一步升级完善,使射波刀的临床治疗日臻完善。射波刀无须使用金属头架或体架,它采用计算机立体定位导航和自动跟踪靶区技术,是新型的大型立体定向放射治疗设备。射波刀由直线加速器、机器人机械臂(Robot Arm)、治疗床、治疗计划系统、靶区定位追踪系统(target localization system)、呼吸追踪系统、计算机网络集成与控制系统组成(如图1和图2)。2006年9月,射波刀的治疗床改进为机器人控制床,准直器的更换从人工改为电脑自动辨认与更换,地面上处于相互垂直位置的非晶硅影像板(X线数码摄像机)被改进到地面以下,使射波刀的照射节点有所增加,特别是Multiplan剂量计划系统的问世,使射波刀治疗进入一个崭新的时代。Accuray公司把新一代的射波刀称为第四代(G4)。第四代射波刀与目前使用的第三代(G3)射波刀在软件上无显著的技术差异,但是治疗流程更加合理。射波刀的问世使放射外科治疗的解剖范围从脑部扩展到全身,它不仅可以治疗颅内肿瘤,还可以治疗颅底肿瘤、头颈部肿瘤、脊髓肿瘤、脊柱肿瘤、肺部肿瘤、胰腺肿瘤、肝脏肿瘤、肾脏肿瘤、前列腺肿瘤、妇科肿瘤、骨科肿瘤。
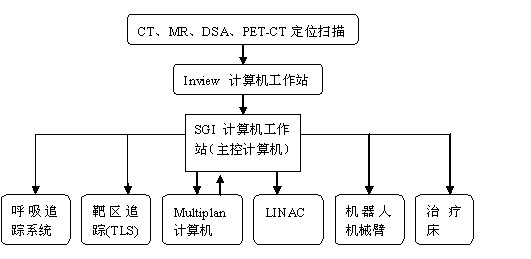
图1:Cyberknife计算机网络集成与控制示意图,Cyberknife主控计算机(SGI)控制着呼吸追踪计算机、TLS、机器人机械臂、直线加速器(LINAC)、治疗床,与Multiplan计算机(治疗计划系统)互联。
图2:射波刀的外形
二、 射波刀的组成:
1、直线加速器: 射波刀使用一个紧凑型、能产生6 MeV X射线和电子束的轻型直线加速器,直线加速器安装在由机器人控制的机械臂上。该直线加速器配有12个准直器,准直器直径从5mm到60mm。
2、机器人机械臂(Robot arm):机器人机械臂头端上安装有直线加速器,它带动直线加速器围绕患者在前、后、左、右、上、下六度空间自由转动,按照计算机预设的路线,机械臂可将直线加速器调整到101个位置(或节点),在每个节点处可以从12个角度投照射线,因此提供多达1212个方位发出射线。每到一预设治疗点,机械臂停止运动,直线加速器对准靶区投照相应的放射剂量。
3、治疗床:第三代射波刀的治疗床由计算机程序和电动控制,可以在五度空间自由移动,即X轴、Y轴、Z轴方向移动、头部倾斜和治疗床左右倾斜,但是治疗床的头部不能在水平位左右转动。第四代射波刀的治疗床由机器人控制,可以在六度空间自由移动。
4、 靶区定位(影像)追踪系统 (target localization system):传统放射外科使用立体定向架固定患者头部,使脑组织与定向架之间产生相对应的三维坐标关系,在治疗中立体定向架确保了射线的精确投照。射波刀使用人体骨骼结构作为参考框架,颅内病灶与颅骨之间产生固定的对应关系。靶区定位(影像)追踪系统是利用天花板上安装的两组诊断X射线球管和安装于患者两侧地面上的非晶体硅摄像机(影像板)组成。两组X射线球管发出的低能X线相互垂直,交叉穿过头颅(或患者肿瘤的治疗部位),摄像机获得颅骨的数字图像,并将影像资料传输到数据处理系统(image processing system, IPS),计算机与事先CT扫描获得的颅骨数字重建图像 (DDR)相比较,首相确定颅骨的精确位置,然后得出治疗靶目标(病灶)的精确位置。靶区定位追踪系统使用4套计算机软件,治疗颅内病变时,使用6维颅骨追踪软件;治疗脊髓、脊柱及其周围肿瘤时,使用Xsight Spine(脊柱追踪软件);治疗部分周围型肺癌时,使用Xsight Lung (肺部追踪软件);治疗随呼吸运动的肿瘤时或需要埋置金标时,使用金标追踪和呼吸追踪系统。
5、治疗计划系统:治疗计划系统由计算机工作站和治疗计划软件组成,早期的治疗计划软件为TPS ( treatment planning system), TPS安装在图形处理工作站上(SGI)。这套软件操作笨拙,设计的治疗计划欠完美,只能接受CT图像,不能将CT图像融合到MRI、PET-CT和DSA图像上。2006年诞生的Multiplan治疗计划软件,使医生可以设计出精美的治疗计划。虽然治疗计划系统只能在CT图像上进行,但是CT影像能够与MRI影像融合,用于获得精细的软组织图像。病人治疗前,先作CT和MRI定位,将定位影像传输到计算机内。医生先勾画出计划治疗的肿瘤和重要器官,然后设置中心点(align center),最后选择准直器并给出肿瘤和重要器官的剂量要求,计算机能自动设计一个满足设定条件、适形满意、剂量分布均匀、照射范围与肿瘤形状几乎吻合的治疗计划。根据治疗的需要,医生可设计单次治疗,也可设计分次治疗(Hypofractoinated cyberknife radiosurgery)。射波刀治疗计划系统不仅具有常规的正向治疗计划,而且还有任意形状逆向治疗计划。正向治疗计划是医生根据病灶的大小和形状,选择相应的准直器和照射方式逐步设计出一个和病灶形状几乎一样的照射形状,然后给出周边剂量和中心剂量。逆向治疗计划是医生先勾画出计划照射的靶区以及给出靶区和重要器官的剂量要求,计算机自动设计一个满足设定条件的治疗计划。射波刀的正向治疗计划远不如伽玛刀的治疗计划系统。但是它可设计等中心照射、非等中心照射,它既可单次治疗,也可分次治疗,兼容放射外科和放射治疗两种功能。
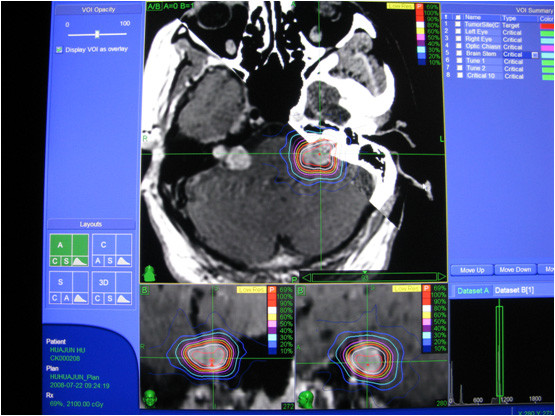
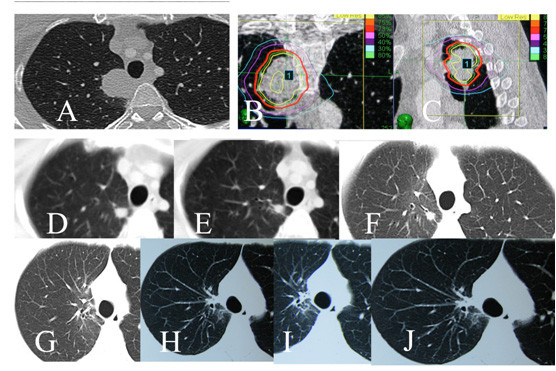
图3:双侧听神经瘤患者,射波刀分3次治疗左侧听神经瘤,大图为CT和MRI融合图像,69%的等剂量曲线覆盖肿瘤,等剂量曲线从内向外依次为90%,80%,69%,60%,50%,40%,30%,20%,10%。小图为MRI的冠状位和矢状位
6、呼吸追踪系统:当治疗肺部肿瘤或受呼吸运动影响的肿瘤(肝癌、胰腺肿瘤等)时,肿瘤随着病人的呼吸而上下左右运动。治疗这些体部肿瘤之前,需要向肿瘤内或周围放置金标(由黄金制成的,长5mm,直径0.8mm的圆柱体称为金标),金标放置5-7天后才能实施射波刀治疗。呼吸追踪是让病人穿上胸前带有发红光二极管的背心,呼吸追踪摄像机通过捕捉二极管的运动获得肺部的呼吸运动节律,计算机建立呼吸模型。治疗时,通过追踪金标的位置获得肿瘤的精确位置,同时计算机根据呼吸节律,自动微调机器人机械臂,让射线始终精确瞄准病灶。
7、计算机网络集成与控制系统:射波刀拥有一个计算机工作站(SGI),SGI计算机通过网络控制机器人机械臂、控制直线加速器何时投照射线、治疗床的移动和治疗靶区位置的追踪。此外,治疗时获得的骨骼图像与定位图像的自动比对均在SGI计算机掌控下自动进行。
8、射波刀治疗的精确度:早期三代射波刀头颅追踪的精确度为0.6±0.3mm,当头颅CT扫描层厚为1.25mm时,射波刀总体误差为1.1±0.3mm。目前头颅CT扫描层厚为1mm,使用六维颅骨追踪技术,治疗头颅肿瘤的误差为0.44±0.12mm,使用金标追踪技术时的误差为0.29±0.1mm,使用脊柱追踪技术治疗脊柱及其周围肿瘤的误差为0.53±0.16mm。
使用呼吸追踪技术治疗肺癌时,头尾方向的误差0.2-1.9mm,左右方向的误差0.2-1.9mm,前后方向的误差0.2-2.5mm。不使用呼吸追踪系统,头尾方向的平均误差0.1-8.1mm,左右方向的误差0.2-4.5mm,前后方向的误差0.2-4.4mm。
三、射波刀的治疗过程
1、制作面罩或体模:颅内肿瘤患者在作定位扫描之前,需要制作一个无创的网眼热缩面罩,用于固定头部,治疗时防止头部移动。体部肿瘤患者需要制作一个体模,用于固定体部。如果体部肿瘤需要金标定位,在治疗前5天将4-5粒金标(fiducial)植入患者肿瘤内或病灶附近,经过几天的休息,金标维持在相对固定的位置,治疗时利用这些金标获得肿瘤的精确定位。
2、射波刀的定位扫描:颅脑肿瘤或脑血管畸形患者使用颅骨结构作为参考框架,定位扫描时,用热缩面罩将头部固定在特制的CT床板上,CT扫描从头顶部开始(头顶外1厘米),一直扫描到下颌以下,扫描层厚为1-1.25mm。体部肿瘤使用脊柱骨骼结构或金标(fiducial)作为定位参考依据,CT扫描时患者平卧在体模内,扫描层厚1-1.5mm,扫描范围为包括肿瘤在内的整个器官。除了CT扫描外,患者还需要作相应部位的增强MRI扫描,用于图像的融合。脑部AVM患者需要做DSA造影和旋转三维DSA。某些体部肿瘤患者需要PET-CT扫描,用于确定肿瘤的精确位置。将定位片输入到Multiplan计算机(治疗计划计算机)内,然后在计算机上设计治疗计划(等中心照射或非等中心照射)。
3、设计治疗计划:在Multiplan计算机上接收CT和MRI定位影像资料,脑血管畸形患者,还需要接受DSA图像资料。首先融合CT和MRI图像,第二在MRI图像上勾画出肿瘤和重要器官,第三选择肿瘤的追踪方式(头颅追踪、脊柱追踪、肺部追踪联合呼吸追踪、金标追踪联合呼吸追踪),第四设置中心点(align center),最后按照病灶的性质、部位和病灶周围是否有重要结构,选择准直器的大小、射线强度、靶区范围、剂量分布、治疗剂量和其它参数,计算机能自动设计一个满足设定条件、适形满意、剂量分布均匀、照射范围与肿瘤形状几乎吻合的治疗计划。治疗计划设计完毕,将治疗计划保存并传输到射波刀SGI计算机上(射波刀主控计算机)。
4、实施治疗:
头部肿瘤的治疗:患者平卧在治疗床上,平卧的姿势与CT扫描时保持一致,并用面罩将头部固定在治疗床上。天花板上的X线球管发射X射线,位于患者两侧的非晶硅摄影机获得一对头颅影像,计算机自动将这对图像与事先CT扫描获得的颅骨数字重建图像 (DDR)进行比对,找到前后左右上下等方位上的误差,技术员通过电脑操作,移动治疗床,使拍摄的头颅图像与数字颅骨图像完全拟合,然后重新拍摄头颅影像,计算机自动比并确认拍摄的头颅图像与颅骨重建图像在6维方向完全拟合在一起(如图4)。此时计算机获得了患者头颅和病灶的初步方位,机械臂将直线加速器旋转到初始坐标位,然后按照程序将加速器围绕着患者旋转到预定节点。直线加速器每到一个节点,机械臂停止运动,此时靶区定位追踪系统立刻获得新的头颅影像,计算机确认目前的头颅影像与治疗开始时影像完全一致。如果头颅有轻微的移动,靶区定位追踪系统立刻计算出移动造成的偏差,并将此偏差传输到机器人机械臂,机械臂微调加速器的方位或射线的入射角度,最后加速器将所需的剂量精确投射到病灶内。如果患者的移动超过计算机自动调整的范围,治疗会紧急暂停(E-stop)。加速器每到一个预定节点,将重复上述影像实时验证步骤。在治疗过程中,X射线球管每10秒钟发射一次,靶区影像追踪系统获取一次影像信息。从摄像到调整数据只需要几秒钟,射波刀基本上做到了在治疗过程中实时跟踪治疗靶区。根据病情需要射波刀可将单次治疗变成多次分割治疗。治疗结束,多数患者无不适,治疗后1周内,少数患者感到疲乏无力,纳差。
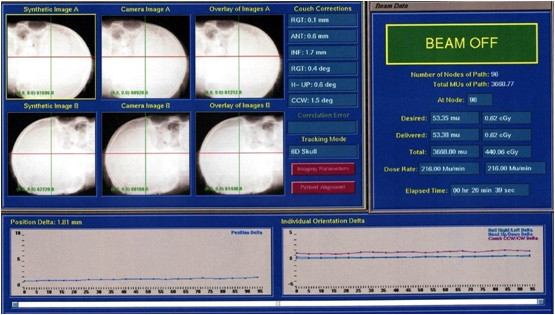
图4:六维颅骨追踪的计算机界面,Synthetic image A和B为CT重建颅骨图像,Camera image A和B为头颅X线数字平片;Overlay of images为两组图像重叠在一起时的结果。
体部肿瘤的治疗:体部肿瘤会随着呼吸节律上下移动,为了使射波刀能够随着患者呼吸节奏给予体部病灶精确照射,需要使用同步呼吸追踪系统,追踪患者的呼吸节律。首先让患者穿上胸部或腹部粘贴发红光二极管的背心平卧在体模内,然后用红光追踪仪(同步呼吸追踪系统,Synchrony)获得呼吸节奏,按照呼吸节律计算机自动建立呼吸模型。治疗体部肿瘤时,射波刀通过拍摄X线片和金标追踪获得体部肿瘤的位置,然后计算机再从呼吸追踪计算机上获取患者的呼吸模型。实施治疗时,机械臂将直线加速器旋转到治疗节点,然后按照呼吸节律微调加速器,使投照的射线始终对准病灶。呼吸追踪技术是一种弹道追踪技术,即在A时间点,肿瘤按照呼吸节律运动到B点,在A时间点,直线加速器将射线精确地投射到B点的位置。按照治疗计划,射波刀重复上述步骤,直到完成所有节点上的照射。
脊柱及其周围肿瘤的治疗:脊柱追踪软件(Xsight Spine)的问世,在治疗脊柱及其周围肿瘤时免除了在脊柱上埋置金标(或金属螺钉)的过程。Xsight Spine可以直接获得脊柱及其周围病灶的精确位置。它是利用计算机软件技术,选取矩形框,框上有81个节点,并形成64个小方格(block)。矩形框覆盖在由CT重建的脊柱骨骼图像上(DDR),由此可获取64个小方格骨表面特征(如图5),并获得81个节点位置。治疗时通过拍摄脊柱X线数字平片,找到相应的锥体,计算机自动比对脊柱X线数字平片上与DDR图像上的64个小方格骨骼表面特征,找到相应的81个节点,然后将获得的两维数据转化为三维数据,获取锥体精确位置,间接获得肿瘤的准确位置,系统误差约0.61mm。脊柱及其周围肿瘤的治疗过程同头颅肿瘤相似,病人平卧在治疗床上的体模内,通过脊柱追踪软件获得肿瘤的准确位置,然后实施治疗。
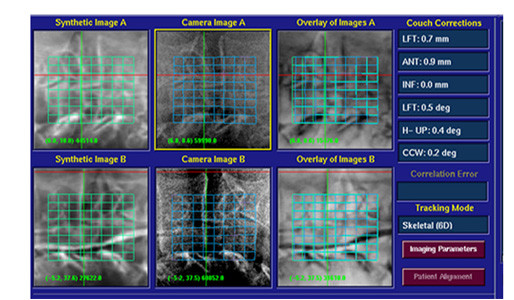
图5:脊柱追踪的计算机界面,Synthetic image为CT重建图像,上面有81个节点组成的64个小方格;Camera image为脊柱X线数字平片;Overlay of images为两组图像重叠在一起时,64个小方格的比对结果。
四、射波刀治疗的适应症及临床应用
1、颅内肿瘤:射波刀主要用于治疗小型或中等大小脑动静脉畸形(AVM)、听神经瘤、三叉神经鞘瘤、中等大小的颅底脑膜瘤、小型垂体瘤、颅内单发或多发转移瘤、其它小型边界清楚的颅内肿瘤以及术后残留的颅内良性肿瘤。对于肿瘤位于深部和重要功能区、常规外科手术难以切除或创伤较大、并发症较高的患者以及高龄、或有系统性疾病不能耐受外科手术的患者,可实施分次射波刀治疗方式(Hypofractoinated cyberknife radiosurgery),来达到控制肿瘤生长提高患者生活质量的目的。在功能神经外科方面,射波刀主要用于治疗三叉神经痛。
射波刀治疗颅内肿瘤的优势在于(1)它既能实施单次治疗又能实施低分割治疗(hypofractionated cyberknife radiosurgery);(2)对于颅底深部、颅颈交界和鼻咽部肿瘤,射波刀的治疗范围广,比传统放射外科有明显的优势;(3)对于恶性或低度恶性肿瘤,肿瘤体积比较大时,射波刀的低分割治疗可以提高照射肿瘤的剂量,降低治疗副反应(如图)。但是,对于小的颅内良性肿瘤,低分割放射外科治疗与单次放射外科治疗之间的差异不明显。下面简介射波刀在临床应用中的一些优势。
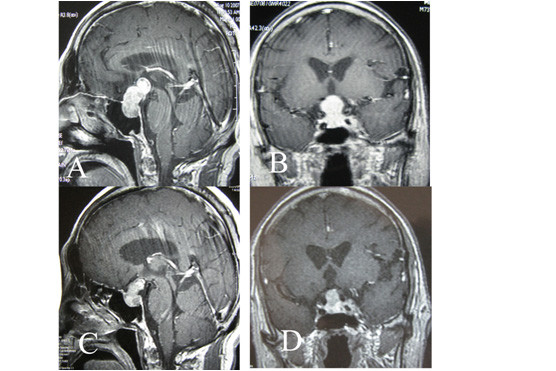
老年颅内良性肿瘤:当患者不能耐受开颅手术时,肿瘤对放射外科治疗相对敏感时,射波刀低分割治疗颅内良性肿瘤有明显优势。将治疗肿瘤的剂量分割成3-5次,可以提高控制肿瘤的剂量,同时减轻副反应。如图6,患者74岁,右侧海绵窦海绵状血管瘤,肿瘤大,不能耐受开颅手术,实施周边剂量21Gy,分割成3次照射,治疗后3个月肿瘤缩小,患者的头痛症状减轻,治疗后14个月,肿瘤进一步缩小。图7为75岁的垂体瘤患者,肿瘤较大,但是患者有内科疾病不能耐受手术,实施周边剂量22.5Gy,分割3次治疗。尽管肿瘤紧贴视神经视交叉,射波刀治疗后,患者视力未受影响,治疗后8个月复查MRI显示肿瘤缩小。
图6:右侧海绵窦海绵状血管瘤(影像学诊断)射波刀治疗前后的比较。A: 射波刀治疗前MRI;B:射波刀治疗后3个月,复查MRI显示肿瘤明显缩小。C和D:治疗后14个月,肿瘤进一步缩小,患者无不适。
图7:高龄垂体瘤患者射波刀治疗前后增强MRI比较。A和B: 射波刀治疗前;C和D:射波刀治疗后8个月,肿瘤缩小,患者视力未受影响。
听神经瘤:中小型听神经瘤是放射外科治疗的良好适应症。伽玛刀治疗听神经瘤比射波刀更具有优势。伽玛刀已经治疗几万例听神经瘤并积累了30多年的临床经验,伽玛刀治疗中小型听神经瘤的疗效已经得到神经外科界的公认。但是,射波刀通过实施低分割照射,在保存有效听力方面比伽玛刀有一定的优势。Ishihara等人应用射波刀治疗38例听神经瘤,他们将治疗剂量分割成1~3次,肿瘤周边平均剂量为17 Gy,有效听力的保存率为93%,无面瘫和三叉神经受损症状。Chang等人报道射波刀分次(staged cyberknife radiosurgery)治疗61例听神经瘤,其随访时间在36个月以上。他们分三次照射肿瘤,每次6~7Gy,肿瘤周边剂量为18~21Gy,肿瘤的控制率为98%。射波刀治疗前,74%的患者拥有有效听力,射波刀治疗后,这些患者的有效听力无减退。
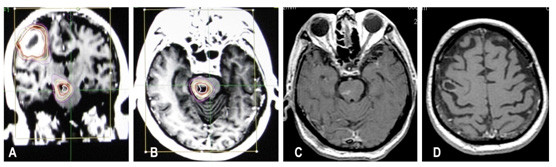
脑干转移瘤:脑干转移瘤占颅内转移瘤的3%左右,但是却严重威胁患者的生命。伽玛刀和常规放疗对脑干转移瘤有较好的控制作用,但是,照射剂量高容易出现脑干水肿,症状加重,照射剂量低,肿瘤控制不佳。射波刀低分割照射,既可以提高照射肿瘤的剂量又可以减轻脑干水肿,治疗后患者症状逐渐改善,脑干转移瘤肿瘤缩小或消失。如图8所示
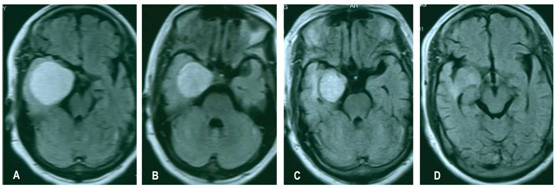
图8:肺癌患者,脑干和右顶叶多发转移瘤。A和B:射波刀治疗计划;C和D射波刀分次治疗后3个月,肿瘤几乎消失,患者原有症状消失。
鞍区靠近视神经视束肿瘤的射波刀治疗:华山医院治疗随访了鞍区和鞍旁肿瘤射波刀分次治疗的初步结果(30例患者),随访结果令人满意。5例视力受影响的患者中,2例视力改善,3例视力保持在治疗前的状态;5例动眼神经受影响的患者中,4例随着肿瘤的缩小,动眼神经受损症状明显改善。其他患者尽管肿瘤靠近视神经、视束或视交叉,但是视力未受影响,表明射波刀分次治疗对保护视神经有一定的优势。5例面部麻木的患者,3例改善。10肿瘤位于海绵窦,射波刀治疗后未出现海绵窦内颅神经受损症状。肿瘤控制情况:25例复查MRI,其中14例肿瘤缩小(垂体瘤3例、脑膜瘤2例、颅咽管瘤4例、海绵窦海绵状血管瘤4例、三叉神经鞘瘤1例),12例肿瘤保持原有大小,其余4例由于随访时间短未复查MRI。
2、青少年鼻咽部纤维血管瘤:青少年鼻咽部纤维血管瘤是好发于青少年的良性肿瘤,但是肿瘤血供丰富,手术切除时出血凶猛,切除不完全肿瘤易复发。由于肿瘤位于鼻咽部,周围结构复杂,是放射外科治疗的良好适应症。由于肿瘤较大,伽玛刀治疗时有时不能完全照射肿瘤。射波刀治疗鼻咽部纤维血管瘤有其独特优越性,它可实施低分割治疗,并获得了良好效果。Deguchi等人报道用射波刀分三次照射鼻咽部纤维血管瘤,照射剂量为45Gy,治疗后7个月肿瘤几乎消失,随访2年未见肿瘤复发。
3、颈静脉孔区肿瘤:颈静脉孔区肿瘤主要包括颈静脉球瘤和颈静脉孔区的神经鞘瘤。虽然手术是主要治疗手段,但是术后的神经受损率高,后遗症较多。伽玛刀放射外科对于肿瘤位置较浅,肿瘤体积不大的患者有良好的治疗作用。当肿瘤较大,位置深时,伽玛刀治疗可能不完全。由于射波刀治疗的解剖范围大,对于鼻咽部、颅底、颈静脉孔区以及颅颈交界部位的肿瘤,射波刀的低分割放疗能完整地照射这些部位的肿瘤,治疗后肿瘤缩小或保持稳定,而副反应较轻。
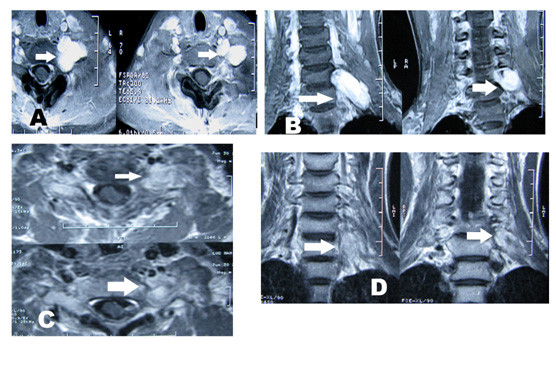
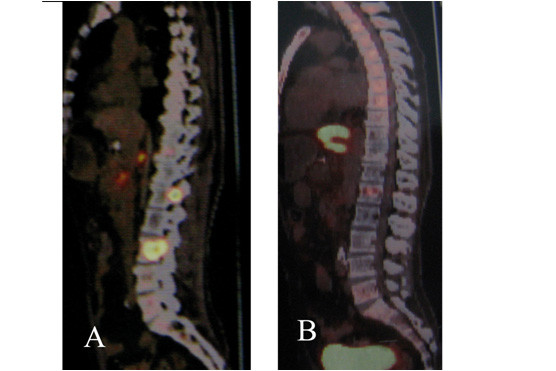
4、脊髓血管畸形、脊柱、椎管内和脊髓肿瘤的射波刀治疗: 脊髓血管畸形主要引起出血、盗血、脊髓压迫和静脉压增高症状,目前的主要治疗方法有介入治疗、显微外科治疗和介入-显微手术联合治疗。射波刀的出现为脊髓血管畸形提供了另一种治疗选择。Sinclair 等人最近报道了射波刀治疗15例脊髓血管畸形的初步结果。他们采用低分割照射(2~5次),经过2~5次的射波刀治疗,病灶周边的平均剂量为20.5Gy,平均随访时间为27个月。随访3年以上的患者中,脊髓血管畸形明显缩小,1例血管畸形经DSA证实完全消失。华山医院治疗1例颈段脊髓AVM,治疗后半年症状改善,治疗后1年走路跛行症状消失。椎管内脊髓外良性肿瘤也可选择射波刀治疗,但是当脊髓有受压症状时,最好选择手术治疗。椎管内小的多发神经纤维瘤是射波刀治疗的良好适应证,射波刀治疗后,多数肿瘤得到控制未再增大,1/3肿瘤缩小。椎管外的神经纤维瘤是射波刀治疗的良好适应症,治疗后肿瘤缩小(如图9所示)。脊髓内恶性肿瘤特别是一些转移瘤,除了引起脊髓受压症状外,还因神经根受刺激而产生疼痛症状;虽然常规放疗能在一定程度上起到控制肿瘤减轻疼痛的作用,但其治疗作用有限。射波刀的低分割照射对脊柱转移瘤和脊髓内转移瘤不仅可以起到控制肿瘤生长(或使肿瘤缩小),还可以明显减轻疼痛,改善患者的临床症状(如图10)。
5、神经系统以外肿瘤的射波刀治疗:射波刀除了治疗神经系统肿瘤和血管畸形外,目前它主要应用于全身肿瘤的放射外科治疗。根据文献报道,射波刀治疗的多数病例为神经系统以外的肿瘤。射波刀已广泛用于肺癌(如图11)、肝脏肿瘤、肾脏肿瘤、前列腺癌、骨肿瘤和一些妇科肿瘤的放射治疗。
图9:颈6-7椎管外神经鞘瘤(椎管内的肿瘤已经手术切除)射波刀治疗前后MRI。A: MRI水平位,箭头所指处为肿瘤;B: MRI冠状位,箭头所指处为肿瘤。C和D:射波刀治疗后半年,肿瘤缩小,强化减弱。
图10:肝癌脊柱转移,患者疼痛症状明显。A: 射波刀治疗前,PET-CT显示腰1椎根和腰3锥体转移瘤; 射波治疗后一周,疼痛症状消失。B: 射波刀治疗后1月复查PET-CT显示转移瘤病灶的FDG(葡萄糖)摄取变为正常。
图11:晚期肺腺癌患者,因脑部转移瘤行开颅手术,病理诊断为腺癌,肺CT检查发现肺癌,然后射波刀治疗。A、B和C:射波刀治疗前肺部CT, A为水平位,B: 为冠状位,C:为矢状位,图像中的红色曲线为治疗时的等剂量曲线。照射3次,每天1次,每次12Gy。DE:治疗后2月,肿瘤缩小为小的结节。FG: 治疗后5个月,肿瘤几乎消失;HIJ: 治疗后7个月,肿瘤消失。
射波刀治疗适应证
一、颅内病变
1、颅内血管畸形:射波刀主要用于治疗脑动静脉畸形(AVM)和海绵状血管瘤。
2、.听神经瘤:中小型听神经瘤(直径<3cm)可首选射波刀治疗,手术后残留或术后复发听神经瘤也是射波刀治疗的良好适应证。部分大型听神经瘤(直径>30mm)患者,如果高龄或有手术禁忌证时仍可考虑射波刀治疗。
3、脑膜瘤:小型脑膜瘤、手术后残留或复发脑膜瘤以及海绵窦、颅底等部位的中小型脑膜瘤均是射波刀治疗的良好适应证。部分术后残留的大型脑膜瘤仍可射波刀治疗。
4、垂体瘤:小型垂体瘤离开视神经、视交叉、视束的距离大于3mm均可射波刀治疗。手术后残留垂体瘤,特别是肿瘤位于海绵窦或紧贴视神经也是射波刀的良好适应证。
5、三叉神经鞘瘤:中小型三叉神经鞘瘤和部分大型三叉神经鞘瘤。
6、脊索瘤:中小型、部分大型脊索瘤及术后残留复发脊索瘤均可射波刀治疗。
7、血管母细胞瘤:小型血管母细胞瘤及术后残留和复发者。
8、颅内转移瘤:颅内单发(肿瘤直径<3.5cm)或数个中小型多发转移灶(一般情况下病灶数<5个,少数情况下可多于5个),颅内压增高症状不严重时,均可行射波刀治疗。
9、胶质瘤:(1)恶性胶质瘤手术后放疗,联合射波刀加量治疗;〔2〕复发胶质瘤的射波刀治疗;(3)低度恶性胶质瘤或偏良性胶质瘤的射波刀治疗,小的低度恶性胶质瘤如星形细胞瘤I级、室管膜下室管膜瘤或偏良性胶质瘤如毛细胞型星形细胞瘤、室管膜下巨细胞型星形细胞瘤、中央神经细胞瘤以及脑干内边界清楚小的胶质瘤均可尝试首选射波刀治疗。
10、颅咽管瘤:术后残留或复发的颅咽管瘤
11、松果体区肿瘤
12、颈静脉孔区肿瘤(颈静脉球瘤和神经鞘瘤)
13、三叉神经痛
14、及鼻咽癌颅底转移等
15、颅内其他小型肿瘤
二、头部肿瘤:鼻咽癌、眼眶肿瘤、头颈部恶性肿瘤及复发肿瘤
三、脊髓脊柱病变
1、脊髓血管畸形
2、脊髓胶质瘤
3、椎管内小的神经鞘瘤
4、椎管外神经鞘瘤
5、脊柱转移瘤
四、体部肿瘤
1、肺癌、肺部转移瘤、纵膈肿瘤及纵膈转移瘤。
2、肝癌、胆囊癌、胆管癌、肝脏转移瘤。
3、肾脏肿瘤及肾上腺转移瘤
4、前列腺癌
5、胰腺癌
6、骨肿瘤
7、腹腔内淋巴结转移。
8、盆腔内肿瘤局部复发或盆腔内淋巴结转移